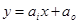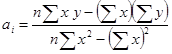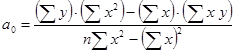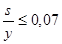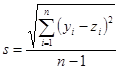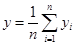Anlage 9
Bestimmung des von Gebrauchsgegenständen aus Kunststoff in Lebensmittel übergegangenen Vinylchlorids
1. | ZWECK UND ANWENDUNGSBEREICH | |||
. | Die Methode ermöglicht die Bestimmung des Gehalts von Vinylchlorid in Lebensmitteln | |||
2. | PRINZIP | |||
Der Gehalt von Vinylchlorid (VC) in Lebensmitteln wird mittels Gaschromatographie unter Anwendung der “Headspace"-Technik bestimmt. | ||||
3. | REAGENZIEN | |||
3.1. | Vinylchlorid (VC), Reinheit mehr als 99,5% (v/v); | |||
3.2. | N,N-Dimethylacetamid (DMA), frei von Verunreinigungen, mit gleicher Retentionszeit - unter den Versuchsbedingungen - wie VC oder der interne Standard (3.3); | |||
3.3. | Diethylether oder cis-2-Buten in DMA (3.2) als Lösung für den internen Standard. Der interne Standard darf keine Verunreinigung mit gleicher Retentionszeit unter Versuchsbedingungen wie VC enthalten; | |||
3.4. | Destilliertes oder entmineralisiertes Wasser entsprechender Reinheit. | |||
4. | APPARATIVES | |||
Anmerkung: | ||||
Instrumente und Geräteteile werden nur dann aufgeführt, wenn sie spezieller Art sind oder besondere Spezifikationen erfordern. Das Vorhandensein der üblichen Laborgeräte wird vorausgesetzt. | ||||
4.1. | Gaschromatograph mit automatischer “Headspace"-Vorrichtung oder einer Vorrichtung für manuelle Probeeingabe; | |||
4.2. | Flammenionisationsdetektor oder andere unter Punkt 7 genannte Detektoren; | |||
4.3. | Gaschromatographiesäule | |||
Die Säule muss die vollständige Trennung des Luft-Peaks, des VC-Peaks und des Peaks des internen Standards, falls ein solcher verwendet wird, ermöglichen. | ||||
Ferner muss die Kombination der Systeme nach 4.2 und 4.3 so beschaffen sein, dass das mit einer Lösung von 0,005 mg VC/l DMA oder 0,005 mg VC/kg DMA erhaltene Signal mindestens fünfmal so stark ist wie der Untergrund. | ||||
4.4. | Fläschchen mit Silicon oder Butylkautschuk-Septen für die Proben | |||
Bei manuellen Verfahren kann die Probenahme aus dem Kopfraum (“Headspace") mit Hilfe einer Spritze die Bildung eines Teilvakuums im Fläschchen zur Folge haben. Für manuelle Verfahren mit Fläschchen, die vor der Probenahme nicht unter Druck gesetzt worden sind, wird deshalb die Verwendung größerer Fläschchen empfohlen. | ||||
4.5. | Micro-Injektionsspritzen; | |||
4.6. | Gasdichte Spritzen für manuelle “Headspace"-Probenahme; | |||
4.7. | Analysenwaage mit 0,1 mg Ablesegenauigkeit. | |||
5. | VERFAHREN | |||
VORSICHT: VC ist ein gefährlicher Stoff und bei Raumtemperatur gasförmig; die Lösungen sollten deshalb in einem gut gelüfteten Abzug zubereitet werden. | ||||
Anmerkung: | ||||
- | Verluste von VC oder DMA sind möglichst zu vermeiden; | |||
- | bei manueller Probenahme sollte ein interner Standard (3.3) verwendet werden; | |||
- | bei Verwendung eines internen Standards ist während des ganzen Verfahrens die gleiche Lösung nach 3.3 zu verwenden. | |||
5.1. | Herstellung der VC-Standardlösung (Lösung A) | |||
5.1.1. | Konzentrierte VC-Standardlösung (zirka 2 000 mg/kg) | |||
Ein passender Gasbehälter wird auf 0,1 mg genau gewogen, eine bestimmte Menge (zB 50 ml) DMA (3.2) eingefüllt und erneut gewogen. Dann wird eine bestimmte Menge (zB 0,1 g) flüssiges oder gasförmiges VC (3.1) langsam zu dem DMA hinzugegeben. Die Zugabe des VC kann auch durch Hineinspülen erfolgen, sofern eine Vorrichtung angewandt wird, mit der DMA-Verluste vermieden werden. Dann wird erneut auf 0,1 mg genau gewogen. Zur Einstellung des Gleichgewichts wartet man zwei Stunden ab. Sofern interner Standard verwendet wird, ist der konzentrierten VC-Standardlösung soviel interner Standard hinzuzufügen, dass deren Konzentration der nach (3.3) hergestellten entspricht. Die Standardlösung wird im Kühlschrank aufbewahrt. | ||||
5.1.2. | Herstellung der verdünnten VC-Standardlösung | |||
Eine eingewogene Menge konzentrierte VC-Standardlösung (5.1.1) wird mit DMA (3.2) oder dem internen Standard (3.3) bis zu einem bekannten Volumen oder Gewicht verdünnt. Die Konzentration der daraus resultierenden verdünnten Standardlösung (Lösung A) wird in mg/l oder mg/kg angegeben. | ||||
5.1.3. | Festlegung der Eichkurve mit der Lösung A Voraussetzung: | |||
- | Die Kurve muss aus mindestens sieben Doppelbestimmungen ermittelt werden; | |||
- | die Wiederholbarkeit des Messwerts (1) darf 0,002 mg VC/l oder kg DMA nicht überschreiten; | |||
- | die Kurve wird nach dem Verfahren der kleinsten Quadrate ermittelt, dh. die Regressionsgerade wird mittels folgender Gleichung berechnet: | |||
wobei | ||||
und | ||||
wobei: | ||||
y = die Höhe oder Fläche des Peaks jeder einzelnen Bestimmung, | ||||
x = die den Messpunkten yi zugehörige VC-Konzentration und | ||||
n = Anzahl der durchgeführten Bestimmungen (n ≥ 14) ist. | ||||
‑ Die Kurve muss linear sein, dh. die Standardabweichung (s) der Unterschiede zwischen den Messwerten (yi) und dem entsprechenden Wert der Regressionsgeraden (zi), geteilt durch den Mittelwert (y) aller Messwerte, darf 0,07 nicht übersteigen. | ||||
Dies ist wie folgt zu berechnen: | ||||
wobei: | ||||
n ≥ 14. | ||||
Man stellt zwei Serien von mindestens je sieben Fläschchen bereit (4.4). In dieses Fläschchen gibt man die notwendigen Mengen verdünnter VC-Standardlösung (5.1.2) und DMA (3.2) oder der Lösung mit dem internen Standard in DMA (3.3), damit die endgültige VC-Konzentration der doppelt hergestellten Lösungen zirka 0, 0,005, 0,010, 0,020, 0,030, 0,040, 0,050 mg/1 oder mg/kg DMA beträgt und jedes Fläschchen das gleiche Gesamtvolumen an Lösung enthält. Die Menge an verdünnter VC-Standardlösung (5.1.2) muss so gewählt werden, dass das Verhältnis des Gesamtvolumens von zugesetzter VC-Lösung (ml) und der Menge (g oder ml) an DMA oder interner Standardlösung (3.3) den Wert 5 nicht überschreitet. Die Fläschchen werden verschlossen und weiter nach 5.4.1, 5.4.3 und 5.4.5 verfahren. Man stellt ein Diagramm her, in dem die Ordinate die Werte der Flächen (und Höhen) der VC-Peaks der beiden Lösungsserien oder das Verhältnis dieser Flächen (oder Höhen) zu denjenigen der entsprechenden Peaks des internen Standards und die Abszisse die Werte der VC-Konzentrationen der beiden Lösungsserien zeigt. | ||||
5.2. | Prüfung auf Richtigkeit der nach 5.1 hergestellten Standardlösungen | |||
5.2.1. | Herstellung einer zweiten VC-Standardlösung (Lösung B) | |||
Das unter Punkt 5.1.1 und 5.1.2 beschriebene Verfahren wird wiederholt, um eine zweite verdünnte Standardlösung mit einer Konzentration in diesem Fall von etwa 0,02 mg VC/l oder 0,02 mg VC/kg DMA bzw. die Lösung für den internen Standard zu erhalten. Diese Lösung ist zu zwei Fläschchen (4.4) hinzuzugeben. Die Fläschchen werden verschlossen; dann wird weiter nach 5.4.1, 5.4.3 und 5.4.5 verfahren. | ||||
5.2.2. | Gültigkeitsprüfung der Lösung A | |||
Wenn der Mittelwert von zwei gaschromatographischen Bestimmungen mit der Lösung B (siehe 5.2.1) nicht mehr als 5% vom entsprechenden Punkt der nach 5.1.3 erhaltenen Eichkurve abweicht, so ist die Lösung A einwandfrei. Ist der Unterschied größer als 5%, so sind alle nach 5.1 und 5.2 hergestellten Lösungen zu verwerfen und das Verfahren von Anfang an zu wiederholen. | ||||
5.3. | Festlegung der “Additions"-Kurve | |||
Anmerkung: | ||||
- | Die Kurve muss aus mindestens sieben Doppelbestimmungen ermittelt werden; | |||
- | die Kurve wird nach dem Verfahren der kleinsten Quadrate ermittelt (siehe 5.1.3, dritter Absatz); | |||
- | die Kurve muss linear sein, dh. die Standardabweichung (s) der Unterschiede zwischen den Messwerten (yi) und dem entsprechenden Wert der Regressionsgeraden (zi), geteilt durch den Mittelwert (y) aller Messwerte, darf 0,07 nicht übersteigen (siehe 5.1.3, vierter Absatz). | |||
5.3.1. | Vorbereitung der Proben | |||
Es ist erforderlich, dass die Probe des zu analysierenden Lebensmittels für das Lebensmittel, wie es dem Analytiker zugeht, repräsentativ ist. Das Lebensmittel sollte deshalb gemischt oder zerkleinert und gemischt werden, bevor die Probe entnommen wird. | ||||
5.3.2. | Verfahren | |||
Man stellt zwei Serien von mindestens je sieben Fläschchen (4.4) bereit. In jedes Fläschchen wird eine Menge von mindestens 5 g der nach der Probeentnahmevorschrift gemäß 5.3.1 entnommenen Probe des Lebensmittels eingegeben. Es muss versucht werden, in jedes Fläschchen die gleiche Menge zu geben. Die Fläschchen werden sofort verschlossen. In allen Fläschchen wird für jedes Gramm Probe 1 ml destilliertes oder entmineralisiertes Wasser mindestens gleicher Reinheit oder ein geeignetes Lösungsmittel hinzugegeben (Anmerkung: für homogene Lebensmittel ist der Zusatz von destilliertem oder entmineralisiertem Wasser nicht erforderlich). Dann werden in jedes Fläschchen entsprechende Volumina der verdünnten VC-Standardlösung (5.1.2), die, wenn es als nützlich erachtet wird, den internen Standard enthält, hinzugefügt; auf diese Weise werden in den Fläschchen VC-Konzentrationen erhalten, die 0, 0,005, 0,010, 0,020, 0,030, 0,040, 0,050 usw. mg/kg des Lebensmittels entsprechen. Es ist sicherzustellen, dass das Gesamtvolumen an DMA oder DMA mit internem Standard (3.3) in jedem der Fläschchen gleich ist. Die Menge an verdünnter VC-Standardlösung (5.1.2) und gegebenenfalls zusätzlichem DMA muss so gewählt werden, dass das Verhältnis zwischen dem Volumen (ml) der VC-Standardlösung und der Menge (g) des in dem Fläschchen enthaltenen Lebensmittels so niedrig wie möglich und höchstens 5 ist. Die Fläschchen werden verschlossen, im Weiteren wird nach 5.4 verfahren. | ||||
5.4. | Gaschromatographische Bestimmungen | |||
5.4.1. | Man schüttelt die Fläschchen, wobei eine Berührung zwischen Inhalt und Septum (4.4) zu vermeiden ist, um eine möglichst homogene Lösung oder Suspension zu erhalten. | |||
5.4.2. | Die verschlossenen Fläschchen (5.2 und 5.3) werden zwei Stunden lang bei 60°+-1 °C ins Wasserbad zur Einstellung des Gleichgewichts gestellt. | |||
5.4.3. | Den Fläschchen wird eine Headspace-Probe entnommen. Bei manueller Probeentnahme ist darauf zu achten, dass eine reproduzierbare Probe entnommen wird (siehe 4.4); insbesondere sollte die Injektionsspritze auf die Temperatur der Probe vorgewärmt werden. Man misst die Fläche (oder Höhe) des dem VC entsprechenden und - falls miteingegeben - des dem internen Standard entsprechenden Peaks. | |||
5.4.4. | Die erhaltenen Werte werden in ein Diagramm übertragen, in dem auf der Ordinate die Flächen (oder Höhen) der VC-Peaks oder das Verhältnis der Flächen (oder Höhen) der VC-Peaks zu den Flächen (oder Höhen) der Peaks des internen Standards und auf der Abszisse die Werte der zu den in jedes Fläschchen (kg) gewogenen Probemengen des Lebensmittels hinzugefügten VC-Mengen (mg) eingetragen werden. Der Schnittpunkt mit der Abszissenachse des Diagramms wird gemessen. Der so erhaltene Wert ist die VC-Konzentration in der zu untersuchenden Lebensmittelprobe. | |||
5.4.5. | Überschüssiges DMA ist gegebenenfalls in geeigneter Weise aus der Säule (4.3) zu entfernen, sobald die DMA-Peaks auf dem Chromatogramm erscheinen. | |||
6. | ERGEBNISSE | |||
Als Konzentration des von den Gebrauchsgegenständen aus Kunststoff an die Lebensmittel abgegebenen Vinylchlorids, ausgedrückt in mg/kg, gilt definitionsgemäß der Mittelwert von zwei Bestimmungen (siehe Punkt 5.4) unter der Voraussetzung, dass dem Wiederholbarkeitskriterium gemäß Punkt 8 entsprochen wird. | ||||
7. | BESTÄTIGUNG DES VC | |||
Übersteigt das nach Punkt 6 von Gebrauchsgegenständen aus Kunststoff an die Lebensmittel abgegebene VC das in § 5 Abs. 4 festgelegte Kriterium, dann sind die bei jeder der zwei Bestimmungen (5.4) erhaltenen Werte nach einem der drei nachstehenden Verfahren zu bestätigen: | ||||
I. | Verwendung mindestens einer anderen Säule (4.3) mit einer stationären Phase unterschiedlicher Polarität. Dieses Verfahren ist fortzusetzen, bis ein weiteres Chromatogramm erhalten wird, auf dem keine Überlappung des VC-Peaks und/oder des Peaks des internen Standards mit Bestandteilen des Lebensmittels festzustellen ist; | |||
II. | Verwendung eines anderen Detektors, zB des Detektors zur Bestimmung der mikroelektrolytischen Leitfähigkeit; | |||
III. | mittels Massenspektrometrie. Wenn in diesem Fall Molekularionen mit den Massen (m/e) 62 und 64 im Verhältnis von 3 : 1 gefunden werden, so kann dies mit hoher Wahrscheinlichkeit als Bestätigung der Anwesenheit von VC betrachtet werden. Im Zweifelsfall ist das gesamte Massenspektrum zu prüfen. | |||
8. | WIEDERHOLBARKEIT | |||
Die Differenz der Ergebnisse zweier Bestimmungen (5.4), die gleichzeitig oder unmittelbar nacheinander an derselben Probe vom selben Analytiker unter gleichen Bedingungen durchgeführt worden sind, darf 0,003 mg VC/kg des Lebensmittels nicht überschreiten. | ||||
Fassung zuletzt geändert durch BGBl. II Nr. 452/2006
Zuletzt aktualisiert am
25.04.2017
Gesetzesnummer
20002952
Dokumentnummer
NOR40085130
Zusatzdokumente: image001, image002, image003, image004, image005, image006
Lizenziert vom RIS (ris.bka.gv.at - CC BY 4.0 DEED)